Хроническая сердечная недостаточность (ХСН) является завершающей стадией целого ряда заболеваний сердечно-сосудистой системы. Она развивается у больных ишемической болезнью сердца, гипертонической болезнью, миокардитами, эндокардитами, перикардитами и другими заболеваниями. Частота ХСН в последние годы непрерывно растет и составляет около 2% взрослого населения (Кушаковский М.С., 1998; Обрезан А.Г., Вологдина И.В., 2002). С ней связан прежде всего высокий уровень летальности, инвалидизации больных, особенно при развитии высоких функциональных классов. Это делает проблему изучения патогенеза, диагностики ХСН одной из наиболее актуальной в современной практической и теоретической кардиологии.
В настоящее время хронические заболевания сердца часто рассматривают как факторы риска ХСН, а само ее проявление – нозологической формой (Обрезан А.Г., 2005). Такой утилитарный подход хотя и выделяет проблему ХСН, не раскрывает сущности этого процесса и не решает вопросов ее профилактики и раннего лечения.
Появившийся в литературе термин «декомпенсация ХСН» как естественное прогрессирование болезней сердца (Белоусов Ю.Б., Ерофеева С.Б., 2004) представляется некорректным, поскольку декомпенсация означает крайнее выражение нарушений деятельности организма, органа или системы, а отнюдь не болезни или ее осложнения. ХСН есть проявление декомпенсации работы сердца. Поэтому исследование этого процесса должно строится не столько на «факторах риска», во многом предположительных, сколько на точном представлении о механизмах становления и развития патологических процессов (Саркисов Д.С., 2000).
Чтобы понять механизм возникновения и развития ХСН, необходимо четко представлять ход патологических процессов, приводящих организм к данному состоянию. Известно, что с самого начала действия патогенного раздражителя в организме происходит повреждение клеточных и тканевых структур и включение компенсаторно-приспособительных реакций на всех уровнях, включая внутриклеточный, что проявляется в регенерации и гиперплазии клеточных органелл (Саркисов Д.С., 1987).
Термин «компенсаторно-приспособительные реакции», так широко применяемый в медицине, с биологической точки зрения, не совсем удачен, так как в организме все реакции являются адаптивными (Грант В., 1991), в том числе и компенсаторные. Они участвуют в обеспечении длительного сохранения гомеостаза организма, т.е. нормального функционирования при непрерывно нарастающих морфологических изменениях органов и тканей. Поэтому правильнее говорить не о компенсаторно-приспособительных, а о компенсаторных реакциях.
В основе компенсаторных реакций лежат регенераторно-гиперпластические процессы, которые обусловлены активацией генного аппарата. В поврежденных тканях с высокой митотической активностью происходит репликация ДНК и усиленная регенерация клеточного пула вовле-ченных в патологический процесс органов. В поврежденных тканях с низкой митотической активностью наблюдается синтез РНК на части матриц ДНК и гиперплазия внутриклеточных и клеточных структур (Маленков А.Г., 1989).
Материальной основой компенсаторных реакций сердца является гиперплазия кардиомиоцитов и гипертрофия органа, а также включение механизма Франка-Старлинга. Очаги же некроза сердечной мышцы замещаются соединительной тканью, а функция погибших элементов нормализуется за счет гиперплазии миокардиальных клеток в оставшейся массе органа. Независимо от то-го, какие причины вызвали повреждение структур компенсаторные реакции при этом будут однотипны.
За счет гиперплазии оставшихся неповрежденными кардиомиоцитов сердце обеспечивает на какое-то время нормальное кровообращение в организме. Однако продолжающееся действие повреждающих факторов способствует дальнейшей гибели функционирующих клеток. Гипертро-фированная ткань в силу того, что она хуже кровоснабжается и иннервируется, при повышенной нагрузке быстрее утрачивает нормальные функциональные свойства. В результате этого на каком-то этапе компенсаторные возможности исчерпываются и развивается декомпенсация, которая проявляется снижением инотропной функции сердца и развитием сердечной недостаточности.
С этих позиций нами была предпринята попытка изучения механизмов становления и этапов развития ХСН у больных ИБС и ГБ.
Материалы и методы исследования
В исследование было включено 166 больных. Мужчины составили 85%, женщины - 15%. Все больные были разделены на три группы. Формирование пациентов по группам соответствовало делению больных с ХСН на стадии А, В и С по классификации Американской Коллегии Кардиологов и Американской Коллегии Сердца (АСС/АНА, 2001). Первую группу (стадия «А» ХСН) составили 33 больных, у которых отмечались заболевания сердечно-сосудистой системы (ГБ и ИБС), без соответствующего структурного или функционального ремоделирования сердца и при отсутствии в прошлом и настоящем каких-либо признаков сердечной недостаточности. Вторая группа (стадия «В» ХСН) представлена 41 больным с отчетливыми признаками гипертрофии мышцы сердца и дилатации полостей, но без явных субъективных признаков сердечной недостаточности. В третью группу (стадия «С» ХСН) включены 92 больных с признаками ХСН, которые выявлялись при обычной физической нагрузке и развивались на фоне структурного или функционального ремоделирования сердца. Наличие ХСН и функциональный класс определяли с помощью клинических методов объективного обследования и пробы с 6-минутной ходьбой.
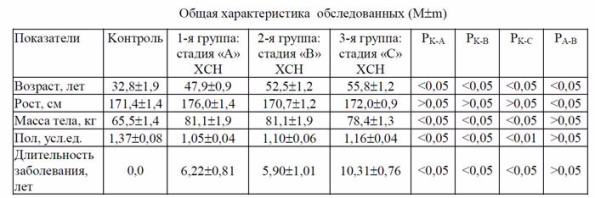
Средний возраст больных в среднем составил 52,5±1,7 лет, у больных 3 группы он был несколько больше, чем у больных 1 и 2 групп (табл. 1). Больные не различались по росту, массе тела и полу. Длительность заболевания оказалась самой большой у больных 3 группы.
Группа контроля в составе 37 человек по половому признаку была идентичной с группами больных, но отличалась по возрасту (32,8±1,9 лет) и массе тела (65,5±1,4 кг). Выбор такой группы контроля обусловлен тем, что лица этого возраста по состоянию здоровья ближе всего находятся к истинной норме и у них, как правило, отсутствуют возрастные изменения, в том числе атеросклероз и артериальная гипертензия (Малов Ю.С., 2003).
Таблица 1.
Обследование больных и здоровых включало общее клиническое и лабораторное исследование, запись ЭКГ, эхокардиографию, суточное мониторирование ЭКГ, допплерографию сонных, сонных, плечевых и бедренных артерий, а у больных ГБ – дополнительно мониторирование АД.
При эхокардиографии выполняли морфометрию миокарда, полстей сердца. Для оценки диастолической функции левого желудочка (ЛЖ) в режиме импульсной допплерографии изучались следующие показатели трансмитрального кровотока: максимальная скорость раннего диастолического кровотока (VЕ), максимальная скорость потока предсердной систолы (VА), их соотношение, время изоволюмического расслабления.
При дуплексном сканировании и допплерографии артерий оценивали стандартные морфологические показатели и параметры внутрисосудистого кровотока.
Для более детальной оценки центральной и периферической гемодинамики был применен метод изучения отношений величин показателей, характеризующих структуру и функции сердца. Отношение структур миокарда является главным внутренним параметром нормального функционирования сердца (Меерсон Ф.З., 1977). Это отношение у здоровых людей подчиняется правилу «золотого сечения» (0,382, 0,618, 1,618 и т.д.). В таком же соответствии находятся и некоторые показатели структуры и функции сердца. Изучены отношения конечных систолического и диастолического размеров ЛЖ, толщины задней стенки в систолу и диастолу, объема левого желудочка в систолу к ударному объему, и последнего к диастолическому объему, систолического АД к диастолическому АД.
Статистическую обработку материала проводили, используя пакет программ Statistic for Windows, 6.0. Достоверность межгрупповых различий средних величин оценивали при помощи критерия t Стьюдента, разницу между результатами считали достоверной при р<0,05. Корреляционные зависимости определяли с использованием коэффициента Пирсона.
Результаты исследования
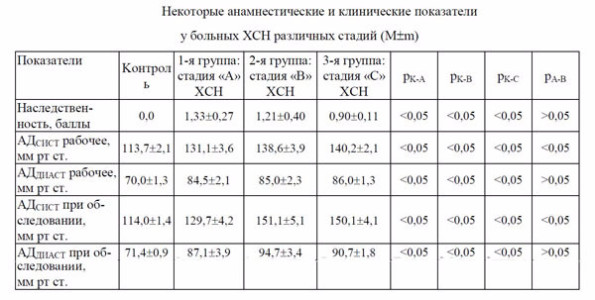
Некоторые анамнестические и клинические показатели у больных ХСН различных стадий представлены в таблице 2. Нами выявлены достоверные различия между пациентами изучаемых групп и здоровыми людьми по большинству показателей, характеризующих уровни «рабочего», максимального за время заболевания и измеряемого при настоящем обследовании АД.
Таблица 2.
Таким образом, прогрессирование артериальной гипертензии может рассматриваться как достоверный фактор риска субъективно-неманифестированного ремоделирования сердца и несомненного появления, в дальнейшем, симптомов ХСН.
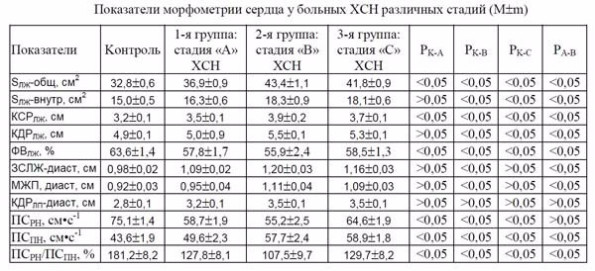
Анализ полученных данных, отражающих как морфологические, так и функциональные изменения, показал определенную динамику нарушений структуры функции сердца у больных разных групп (табл. 3).
Таблица 3.
Примечание: SЛЖобщ - общая площадь поперечного сечения ЛЖ; SЛЖ-внутр - внутренняя площадь поперечного сечения ЛЖ; МЖП – толщина межжелудочковой перегородки в диастолу (см); ЗСЛЖ – толщина задней стенки ЛЖ в диастолу; КДРЛЖ – конечный диастолический размер ЛЖ; КСРЛЖ – конечный систолический размер ЛЖ; КДРЛП – конечный диастолический размер левого предсердия; ФВЛЖ – фракиця выброса ЛЖ; ПСРН - пиковая скорость трансмитрального кровотока во время раннего диастолического наполнения; ПСПН, пиковая скорость трансмитрального кровотока во время позднего диастолического наполнения; ПСРН/ПСПН – соотношение пиковая скорость трансмитрального кровотока во время раннего и позднего диастолического наполнения; ВИВР - время изоволюмического расслабления ЛЖ.
У больных 1-й группы по сравнению со здоровыми наблюдаются увеличение общей площади ЛЖ, конечного систолического и диастолического размера и систолического объема ЛЖ, умеренное снижение фракции выброса (ФВ), утолщение задней стенки ЛЖ в диастолу, увеличение диаметра левого предсердия (ЛП) в систолу и диастолу, расширение аорты.
Необходимо отметить, что в соответствии с принципом формирования групп у пациентов 1-й группы не отмечено субъективных признаков ХСН.
Больные 2-й группы существенно отличались по значительному числу изучаемых показателей от здоровых людей, но в меньшей степени от больных 1 группы. У них выявлено повышение систолического, диастолического АД, увеличение частоты сердечных сокращений, общей и внутренней площади ЛЖ, его размеров и объемов, минутного и ударного объемов. Установлено дальнейшее снижение фракции выброса, нарастание толщины задней стенки ЛЖ и межжелудочковой перегородки в систолу и диастолу, увеличение размеров ЛП, диаметра и толщины стенки аорты. Для больных этой группы было характерно развитие диастолической дисфункции ЛЖ, что проявлялось уменьшением скорости диастолического потока раннего наполнения и увеличением скорости потока предсердной систолы с нарушением их соотношения. Отмечено увеличение модуля уп-ругости, массы и индекса мышечной массы ЛЖ, которые достоверно превышали подобные пока-затели у больных 1-й группы и отражали развитие гипертрофии и ремоделирования сердца. Не-смотря на приведенные нарушения центральной гемодинамики и структуры сердца, у больных 2-й группы не отмечено субъективных признаков ХСН.
Параметры, отражающие морфологию и функцию сердца, у больных 3 группы достоверно отличались от таковых в контроле и у больных 1 группы. Однако, различия большинства показателей у больных 2 и 3 групп оказались недостоверными. Размеры ЛП, ЛЖ, их объемы в систолу и диастолу, ФВ, АД у больных этих групп были примерно одинаковыми. Все же следует отметить дальнейшее увеличение частоты пульса, минутного объема при наметившейся четкой тенденции к уменьшению массы и индекса массы ЛЖ, толщины задней стенки и межжелудочковой перегородки. На фоне приведенных изменений гемодинамики у больных 3 группы наблюдались признаки ХСН: одышка, утомляемость, акроцианоз, отеки на нижних конечностях, в ряде случаев выслушивались влажные незвучные хрипы в легких.
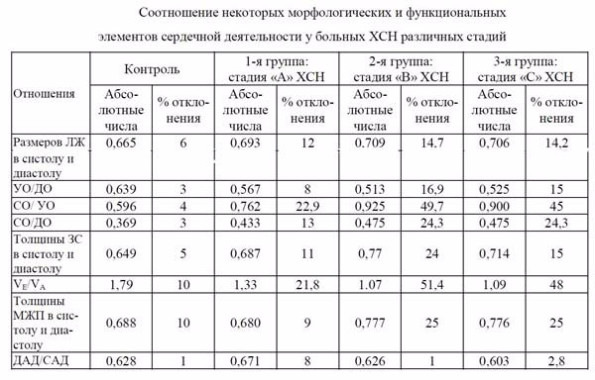
Изучение соотношений некоторых структур сердца и их функций у здоровых обследованных позволило установить закономерности, соответствующие правилам «золотого сечения» (табл. 4).
Таблица 4.
Примечание. ЛЖ – левый желудочек; УО – ударный объем; ДО - диастолический объем ЛЖ; СО – систолический объем ЛЖ; ЗС – задняя стенка ЛЖ; МЖП - межжелудочковая перегородка; VЕ/VА - соотношение скоростей потоков раннего – Е и позднего (А) наполнения ЛЖ; ДАД – диастолическое АД; САД – систолическое АД.
В таком соотношении находятся размеры ЛЖ в систолу и диастолу, толщина задней стенки ЛЖ в разные фазы сердечной деятельности, объемы левого желудочка в систолу и диастолу, ударный и систолический, ударный и диастолический объемы, пиковые скорости трансмитрального кровотока, диастолическое и систолическое АД. Колебания этих отношений находятся в пределах ± 1-6% от золотого сечения и только диапазон колебаний VЕ/VА составлял ± 10%.
У больных всех групп данные закономерности были существенно нарушены. (табл. 4). Характер и степень этих нарушений зависели от выраженности морфологических изменений мышцы сердца. Отчетливые отклонения от «золотого сечения» выявлены уже у больных 1 группы. По большинству показателей эти отклонения составили 10-20%. Величина отклонения этих показателей у них была в 2-4 раза больше, чем в контроле. Максимальные отклонения от величин «золотого сечения» наблюдались у больных 2 группы и составляли 15-50%, что примерно в 3-10 раз больше, чем у здоровых. Из всех показателей более всего от «золотого сечения» отклонялись отношение систолического объема ЛЖ и ударного объема и отношение пиковых скоростей диастолического кровотока.
У больных с ХСН 3-й группы отклонение отношений изучаемых величин от «золотого сечения» достоверно не отличалось от таковых у больных 2 группы. Однако, у них наметилась тенденция к уменьшению этих отклонений. Отношение толщины задней стенки в систолу и диастолу достоверно снизилось, что можно расценить как отражение уменьшения мышечной массы ЛЖ.
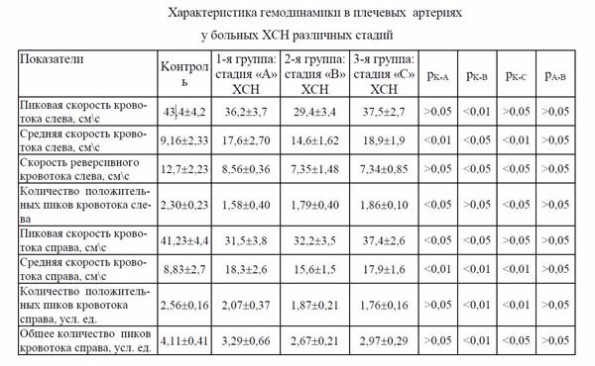
Одновременно с морфофункциональными изменениями в сердце у больных ИБС и ГБ вы-явлены нарушения кровотока по сосудам мышечного и эластического типов (сонные, плечевые и бедренные артерии) (табл. 5).
Эти нарушения в разных сосудах имели однонаправленный характер, хотя в количественном выражении они существенно отличались друг от друга. Следует в первую очередь отметить достоверное снижение пиковых скоростей кровотока по перечисленным артериям. Наибольшее снижение скорости кровотока наблюдалось у больных 3 группы, хотя достоверной разницы в показателях больных обследованных групп не выявлено.
Снижение скорости кровотока по артериям сопровождалось падением минутного объема. У больных 1 группы отмечено резкое снижение минутного объема по всем сосудам. У больных 2 и особенно 3 группы он несколько возрастал, достигая половины от контрольного (p<0,001). На фоне снижения минутного объема происходило увеличение ударного объема. Наиболее отчетливо это проявилось у больных 1 группы, у которых он увеличился в 2 и более раза. У больных 2 группы ударный объем несколько снизился, а у больных 3 группы вновь увеличился.
Таблица 5.
Обсуждение и выводы
Полученные нами данные свидетельствуют о том, что патологический процесс в сердце начинается с повреждения морфологических структур и постепенно прогрессирует. Для поддержания насосной функции сердца организм использует компенсаторные реакции, которые на начальных этапах задействуют механизм Франка-Старлинга и гиперплазию органелл кардиомиоцитов. Это проявляется гипертрофией и умеренной дилатацией полостей сердца и соответствует тоно-генной дилатации по Г.Ф.Лангу. За счет этого происходит восстановление и даже усиление ино-тропной функции сердца, что обеспечивает нормальное кровообращение в органах и тканях. Данное положение подтверждается результатами исследования больных 1-й группы, у которых установлено увеличение размеров и объемов ЛП и ЛЖ, тенденция к гипертрофии ЛЖ. К ранним проявлениям ХСН при ГБ и ИБС следует отнести гипертрофию и дилатацию левого предсердия. По данным П.П. Черныша (2003) эти изменения могут быть обусловлены увеличением объема циркулирующей крови.
Прогрессирование болезни сердца, с одной стороны, сопровождается дальнейшими морфофункциональными изменениями, с другой – включением все новых механизмов компенсации со стороны не только самого сердца, но и других систем, направленных на нейтрализацию и ликвидацию последствий разрушающего действия патогенных факторов. Это отчетливо прослеживается у больных 2 группы, у которых отмечена наибольшая гипертрофия ЛП, межжелудочковой перегородки, ЛЖ, значительное увеличение полостей сердца (его ремоделирование), снижение ФВ, максимальное отклонение отношений структур и функций сердца от «золотого сечения», стойкое повышение АД. Однако насосная функция сердца у этих больных остается на достаточно высоком уровне, обеспечивая достаточное кровоснабжение тканей организма в повседневных условиях. Необходимо подчеркнуть, что у больных 2-й группы уже можно выявить признаки скрытой сердечной недостаточности, о чем свидетельствует увеличение размеров ЛП, ЛЖ, их объемов, времени изометрического расслабления, что соответствует первой стадии сердечной недостаточности (Комаров Ф.И., Ольбинская Л.И., 1978). По нашим данным, важными и ранними показате-лями сердечной недостаточности являются увеличение систолического объема ЛЖ, а также соотношения систолического объема к ударному. Отношение ударного объема ЛЖ к диастолическому (фракция выброса) хотя и отражает степень выраженности СН, но не является столь обязательным признаком этого осложнения. Ударный и минутные объемы сердца менялись мало и даже имели тенденцию к увеличению у больных с сердечно недостаточностью, что не противоречит литературным данным.
Представленные данные позволяют предположить, что у больных 2-й группы компенсаторные возможности сердца практически исчерпаны, поскольку гипертрофия охватывает все мышечные структуры этого органа, а тоногенная дилатация ЛЖ сменяется миогенной. Это предположение, подтверждают результаты исследования больных 3-й группы, у которых наблюдаются явные признаки сердечной недостаточности. Оказалось, что большинство изучаемых показателей у них было таким же, как и у больных 2 группы. Разница по изучаемым показателям между ними не была существенной. В этой связи возникает вопрос, почему же при одинаковых морфологических изменениях в сердце, у одних больных выявляется явная сердечная недостаточность, а у других она отсутствует или проявляется в скрытом виде.
Ответ на этот вопрос, на наш взгляд, могут дать данные об однонаправленности изменений показателей, характеризующих мышечную массу сердца у больных 3-й группы. У них прослеживаются снижение массы миокарда, ИММ ЛЖ, уменьшение толщины задней стенки ЛЖ в систолу и диастолу, межжелудочковой перегородки, задней стенки ЛП. Эти данные говорят о том, что сердце у больных данной группы не способно дальше гипертрофироваться и компенсировать полностью насосную функцию за счет этого механизма. Необходимо отметить, что гипертрофированПолученные нами данные о последовательности развития морфофункциональных нарушений сердца и сосудов у больных ГБ и ИБС позволяют выделить два периода или две стадии тече-ния патологического процесса независимо от того, чем он вызван (нагрузкой давлением или поражением коронарных артерий). Первая стадия характеризуется полной компенсацией инотропной функции сердца, что, вероятно, соответствует НК «0» по Г.Ф. Лангу или «А» стадии по классификации АСС/АНА (2002). Для второй стадии свойственно истощение компенсаторных реакций, т.е. декомпенсация. Она может проявляться различной степенью выраженности. Так, выявленные изменения у больных 2-й группы можно рассматривать как субкомпенсацию или первую степень декомпенсации, которая, как правило, выявляется при повышенной физической нагрузке. У больных 3 группы обнаруженные изменения можно отнести к неполной декомпенсации или к декомпенсации второй степени. Полная декомпенсация, или 3-я степень, свойственна больным с клиническими признаками сердечной недостаточности, проявляющимися в покое.
На основании полученных данных можно сделать вывод, что ХСН есть проявление декомпенсации сократительной функции сердца. Степень выраженности ее отражает тяжесть сердечной недостаточности и прогрессирование патологического процесса, приведшего к ХСН. Она зависит, с одной стороны, от характера течения заболевания, с другой, - от компенсаторного потенциала организма. Чем выше этот потенциал, тем менее выражена ХСН. Выраженность ее также будет уменьшаться при снижении активности патологического процесса спонтанно или под влиянием терапии. Рецидив болезни или неадекватное лечение приводит к нарастанию выраженности декомпенсации, а значит, и тяжести хронической сердечной недостаточности.
Самый дискутабельный вопрос остается в том, можно ли говорить о стадии заболевания, если имеется вероятность обратного развития процесса или повышение степени компенсации. Нам представляется логичным вывод, согласно которому ХСН более целесообразно различать по степени, а вот в отношении стадийности процесса имеются определенные сомнения. По нашим представлениям стадия отражает определенную ступень в развитии болезни, а не ее осложнения. Вероятно, ХСН не только прогрессирует, но может и регрессировать, если в организме сохранились компенсаторные возможности, которые могут быть усилены проводимым лечением.
Учитывая, что ХСН является заключительной стадией, завершающим этапом различных заболеваний сердца, делить ее на подстадии (стадии), по-видимому, не совсем правильно. Хотя в течении ХСН и просматривается некоторая фазность (стадийность), она не является строго закономерной и, в большей мере, определяется прогрессированием основного заболевания. Выраженность ХСН может изменяться как в сторону прогрессирования, так и в сторону регресса в зависимости от характера течения заболевания, компенсаторных возможностей организма и характера проводимой терапии. Действительно, практические наблюдения показывают, что на современном этапе возможно не только снижение функционального класса сердечной недостаточности, но и уменьшение стадии заболевания (хотя и временное). Именно в этой связи ХСН более целесообразно различать не по стадиям, а по степени тяжести или по функциональным классам. Стадия отражает определенную фазу развития болезни, а ее осложнения указывают на степень выраженности (тяжести) патологического процесса и компенсаторные возможности организма. Таким образом, принимая за основу суждение о ХСН как об осложнении болезни сердца, более логично присваивать степень тяжести самому заболеванию или указывать степень компенсации сердечнойинотропной функции. При рассмотрении же ХСН в качестве самостоятельной нозологии, действительно разумно говорить о стадиях или функциональных классах болезни. На настоящем этапе представлений о сердечной недостаточности, а также при двойственности терминологии (ХСН и НК), судить достоверно о стадийности или функциональности этого процесса нельзя. Нельзя не принимать во внимание многочисленные факты, показывающие несомненную роль в патофизиологии сердечной недостаточности параметров периферического кровообращения, состояния тканевой перфузии, степени приспособленности метаболизма тканей к изменившимся условиям системной гемодинамики (Обрезан А.Г., 2005). При таком рассмотрении проблемы более справедлив термин «недостаточность кровообращения». Для упорядочения представлений о стадийности ХСН\НК можно также принять за основу принцип деления на стадии гипертонической болезни, когда возможность нивелирования признаков, относящих болезнь ко 2-й стадии, не принимается во внимание ввиду необходимости медикаментозного вмешательства для регресса этих симптомов.
Литература
- Обрезан А.Г., Вологдина И.В. Хроническая сердечная недостаточность. - С-Пб: «Вита Нова». – 2002. – 320 с.
- Обрезан А.Г. К вопросу о терминологии: «недостаточность кровообращения» или «сердечная недостаточность»? // Медицина XXI век. – 2005. - № 1 (1). – С. 50-54.
- Кушаковский М.С. Хроническая застойная сердечная недостаточность. Идиопатические кардиомиопатии. СПб.: Фолиант. - 1998. - 320 с.
- Белоусов Ю.Б., Ерофеева С.Б. Левосимендан – новый препарат для лечения сердечной недостаточности // Фарматека. – 2004. - № 8. – С. 56-61.
- Саркисов Д.С. Некоторые особенности развития медикобиолоических наук в последние столетия // Клин. Мед. – 2000. - № 7. – С. 4-8.
- Структурные основы адаптации и компенсации нарушенных функций / Под. Ред. Д.С.Саркисова. – М.: Медицина. – 1987. – 100 с.
- Маленков А.Г., Гомеостаз и конвариантная редупликация (Об основах теоретической биологии) // Онтогенез, эволюция, биосфера. – М.: Наука. – 1989. – С. 30-44.
- Малов Ю.С. Биологические основы здоровья и болезней // Вестник Российской Военно-медицинской академии. – 2003. - № 2. – С. 141-146.
- Меерсон Ф.З. Адаптация, дезадаптация и недостаточность сердца. – М.: Медицина. – 1977. – 200 с.
- Комаров Ф.И., Ольбинская Л.И. Начальная стадия сердечной недостаточности. М.: Медицина, 1978.
- Черныш П.П., Малов Ю.С. Использование пропорций «золотого сечения» для диагностики хронической сердечной недостаточности // Кардиология СНГ. – 2003. - № 1. – С. 312.
- Грант В. Эволюционный прогресс (Критический обзор эволюционной теории) // М.: Мир. – 1991.
- ACC/AHA/ Guidelines for the Management of Patients With Chronic Heart Failure 2002 // internet source: www. acc.org.
Источник: Малов Ю.С., А.Г.Обрезан Хроническая сердечная недостаточность – декомпенсация сердечно-сосудистой деятельности \\ Медицина XXI век. – 2006. - №3(4). – С. 53-59.