Хроническая сердечная недостаточность (ХСН) является осложнением многих заболеваний сердечно-сосудистой системы. Наиболее часто ХСН развивается у больных ишемической болезнью сердца (ИБС) (60% всех случаев ХСН), клапанными пороками сердца (14%), дилатационной кардиомиопатией (11%). Артериальная гипертензия (АГ) как основная причина развития ХСН наблюдается всего в 4% случаев, однако она часто сопутствует ИБС и способствует развитию данного осложнения. (1)
Повышение заболеваемости ИБС, ГБ в последние годы способствовало росту и частоты ХСН. Она составила 2% взрослого населения всех стран мира (2, 3, 4). ХСН стала одной из главных причин инвалидизации и смертности больных сердечно- сосудистой патологией, несмотря на достигнутые успехи в их лечении. Это делает проблему изучения патогенеза и диагностики ХСН одной из наиболее актуальных в современной практической и теоретической кардиологии.
Отсутствие четкой ясности о том, что представляет собой ХСН - завершающая стадия хронических заболеваний сердца, проявляющаяся патофизиологическим синдромом, вызванным снижением его насосной функции, или самостоятельная нозологическая форма, сформировавшаяся в результате нейрогуморальных нарушений, находящихся вне зависимости от этиологии поражения (1,3).
Выделение ХСН в нозологическую форму имеет больше практическую направленность, ибо оно облегчает практикующим врачам выбор стандартов лечения данного состояния, но не раскрывает сущности патологического процесса, приводящего к этим изменениям. Хронические заболевания сердечно-сосудистой системы в данной ситуации рассматриваются как «факторы риска», способствующие развитию ХСН.
По-видимому, при решении столь сложной проблемы лучше ориентироваться не на «факторы риска», а на точное представление о механизмах становления и развития патологических процессов.(5).
Хорошо известно, что с самого начала действия патогенного раздражителя в организме происходит повреждение клеточных и тканевых структур и включение компенсаторных реакций на всех уровнях, включая внутриклеточный, что проявляется регенерацией клеток или гиперплазией клеточных органелл, гипертрофией клеток и органа. В основе этого процесса лежит активация генного аппарата клеток (6).
В виду того, что кардиомиоциты не обладают митотической активностью, материальной основой компенсаторных реакций сердца является гиперплазия органелл клеток миокарда и гипертрофия органа, а также включение механизма Франка-Старлинга. Эти реакции поддерживают на должном уровне сократительную функцию сердца, нарушенную гибелью части клеток, на месте которых развивается соединительная ткань, и обеспечивают на какое-то время нормальное кровообращение в организме.
Следует отметить, что независимо от того, какие причины вызвали повреждение структур, компенсаторные реакции будут протекать однотипно. По-видимому, этим можно объяснить единый генез ХСН. Однако гипертрофированная ткань обладает меньшим жизненным потенциалом, так как она хуже кровоснабжается и иннервируется, и при повышенной нагрузке она быстрее утрачивает нормальные функциональные свойства (6). При продолжающемся действии повреждающих факторов происходит гибель функционирующих клеток, компенсаторный резерв постепенно исчерпывается. Это приводит к декомпенсации сердечной деятельности, которая проявляется в первую очередь снижением инотропной функции и развитием сердечной недостаточности.
С этих позиций нами была предпринята попытка изучения механизмов становления и развития ХСН у больных ИБС и ГБ
Материалы и методы исследования
В исследование было включено 166 больных. Мужчины составили 85%, женщины – 15 %.Все больные были разделены на три группы. Формирование пациентов по группам соответствовало делению больных с ХСН на стадии «А», «В» и «С» по классификации Американской коллегии кардиологов и Американской коллегии сердца (АСС/АНА,11). Первую группу (стадия «А» ХСН) составили 33 больных, у которых были выявлены заболевания сердечно- сосудистой системы (ИБС и ГБ) без структурного и функционального ремоделирования сердца и при отсутствии в прошлом и настоящем каких-либо признаков сердечной недостаточности. Вторая группа (стадия «В» ХСН) представлена 41 больным с отчетливыми признаками гипертрофии мышцы сердца и делатации полстей, но без явных субъективных признаков сердечной недостаточности. В третью группу (стадия «С» ХСН) включены 92 больных с признаками ХСН, которые выявлялись при обычной физической нагрузке и развивались на фоне структурного и функционального ремоделирования сердца. Наличие ХСН и ее функциональный класс определяли с помощью методов объективного обследования и пробы с 6-минутной ходьбой.
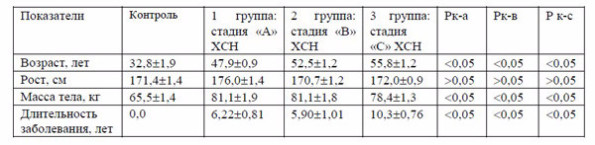
Средний возраст больных составлял 52,5_+1,7 лет, у больных 3 группы он был несколько больше, чем у больных 1 и 2 групп (Табл.1). Больные не различались по росту, массе тела и полу. Однако длительность заболевания оказалась самой большой у больных 3 группы.
Таблица 1. Общая характеристика обследованных
Группа контроля в составе 37 человек по половому признаку была идентичной с группами больных, но отличалась по возрасту (32,8+1,9 лет) и массе тела (65,5+ 1,4 кг). Выбор такой группы контроля обусловлен тем, что лица этого возраста по состоянию здоровья ближе всего находятся к истинной норме и у них, как правило, отсутствуют возрастные изменения, в том числе атеросклероз и гипертензия (7)
Обследование больных и здоровых лиц включало общее клиническое и лабораторное исследование, запись ЭКГ, эхокардиографию, суточное мониторирование ЭКГ, допплерографию сонных, плечевых и бедренных артерий, а у больных ГБ – дополнительное мониторирование. А/Д.
При эхокардиографии выполняли морфометрию миокарда и полостей сердца. Для оценки диастолической функции левого желудочка (ЛЖ) в режиме импульсной допплерографии изучались следующие показатели трансмитрального кровотока: максимальная скорость раннего диастолического кровотока (Ve), максимальная скорость потока предсердной систолы (Va), их соотношение, время изоволюмического расслабления. Стандартные морфологические показатели и параметры внутрисосудистого кровотока оценивали с помощью дуплексного сканирования и допплерографии.
Для более детального исследования центральной и периферической гемодинамики был использован метод, основанный на закономерностях «золотого сечения» (ЗС) и позволяющий выявить соотношение величин, отражающих структуры и функции сердца. Отношение структур миокарда является главным параметром нормального функционирования сердца (8).Это отношение у здоровых людей подчиняется правилу «золотого сечения» и выражается следующими цифрами:0,382, 0,618, 1, 1,618 и т.д. В таком же соответствии находятся и некоторые функции сердца. Изучены отношения конечных систолического и диастолического размеров ЛЖ, толщины задней стенки в систолу и диастолу, объема левого желудочка в систолу к ударному объему, и последнего к диастолическому, систолического к диастолическому А/Д. Статистическую обработку материала проводили, используя пакет программ Statistic for Windows, 6.0. Достоверность межгрупповых различий средних величин оценивали при помощи критерия t Стьюдента, разницу между результатами считали достоверной при р< 0,05. Корреляционные зависимости определяли с использованием коэффициента Пирсона.
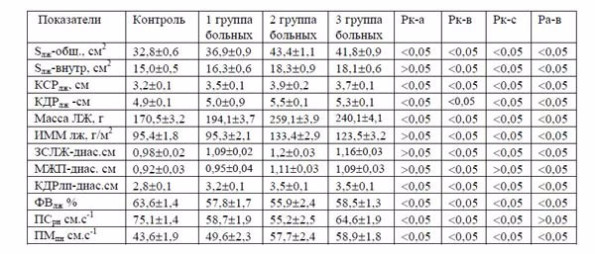
Таблица 2. Показатели морфометрии сердца у больных ХСН различных стадий
Примечание: S лж -общ – общая площадь поперечного сечения ЛЖ; S лж-внутр – внутренняя площадь поперечного сечения ЛЖ; МЖП – толщина межжелудочковой перегородки; ЗСлж – толщина задней стенки ЛЖ в диастолу; КДР ЛЖ – конечный диастолический размерЛЖ; КСРЛЖ – конечный систолический размер ЛЖ; КДРлп – конечный диастолический размер левого предсердия; ФВлж – фракция выброса ЛЖ; ПСрн – пиковая скорость трансмитрального кровотока во время раннего диастолического наполнения; ПСпн – пиковая скорость трансмитрального кровотока во время позднего диастолического наполнения.
Результаты исследования
Анализ полученных данных, отражающих как морфологические, так и функциональные изменения, показал определенную динамику нарушений структуры и функций сердца у больных разных групп (Табл.2).
Из данной таблицы следует, что у больных 1 группы по сравнению со здоровыми наблюдалось увеличение общей площади ЛЖ, конечного систолического и диастолического размера и систолического объема ЛЖ, умеренное снижение фракции выброса (ФВ), утолщение задней стенки ЛЖ в диастолу, увеличение диаметра левого предсердия (ЛП) в диастолу, расширение аорты. Необходимо отметить, что в соответствии с принципом формирования групп у пациентов 1-й группы отсутствовали объективные и субъективные признаки ХСН.
Больные 2 группы существенно отличались по значительному числу изучаемых показателей от здоровых людей, но в меньшей степени от больных 1 группы. У них выявлено повышение систолического, диастолического А/Д, увеличение частоты сердечных сокращений, общей и внутренней площади ЛЖ, его размеров и объемов, минутного и ударного объемов. Установлено дальнейшее снижение фракции выброса, нарастание толщины задней стенки ЛЖ и межжелудочковой перегородки (МП) в систолу и диастолу, увеличение размеров ЛП, диаметра и толщины стенки аорты.
Для больных этой группы характерно развитие диастолической дисфункции ЛЖ, что проявляется уменьшением скорости диастолического потока и увеличением скорости потока предсердной систолы и нарушением их соотношения. Отмечено увеличение модуля упругости, массы и индекса массы ЛЖ, которые достоверно превышают подобные показатели у больных 1 группы, развитие гипертрофии и ремоделирования сердца. Несмотря на приведенные нарушения центральной гемодинамики и структуры сердца, у больных второй группы не выявлено субъективных признаков ХСН.
Параметры, отражающие морфологию и функцию сердца, у больных 3 группы достоверно отличались от таковых в контроле и у больных 1 группы. Различия же большинства показателей у больных 2 и 3 групп оказались недостоверными. Размеры ЛП, ЛЖ, их объемы в систолу и диастолу, ФВ, А/Д у больных этих групп были примерно одинаковыми. Однако следует отметить, что происходило дальнейшее увеличение частоты пульса, минутного объема при наметившейся четкой тенденции к уменьшению массы и индекса массы ЛЖ, толщины задней стенки и межжелудочковой перегородки. При одинаковых показателях нарушения гемодинамики с больными 2 группы у пациентов 3 группы наблюдались признаки ХСН: одышка, утомляемость, акроцианоз, периодически появляющиеся или постоянные отеки на нижних конечностях, в ряде случаев выслушивались влажные незвучные хрипы в легких.
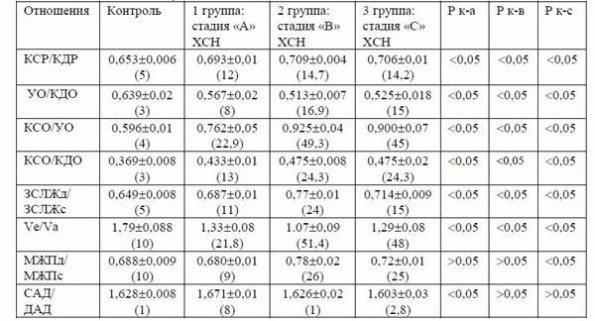
Изучение соотношений некоторых структур сердца и их функций у здоровых лиц позволило установить закономерности, соответствующие правилам «ЗС» (Табл.3). В таком соотношении находились размеры ЛЖ в систолу и диастолу, толщина задней стенки ЛЖ в разные фазы сердечной деятельности, объемы левого желудочка в систолу и диастолу, ударный и систолический, ударный и диастолический объемы, пиковые скорости трансмитрального кровотока, систолическое и диастолическое А/Д. Колебания этих отношений находились в пределах ±1-5% от «ЗС» и только диапазон колебаний Ve/Va составлял ±10%
Таблица 3. Соотношение некоторых морфологических элементов сердечной деятельности у больных ХСН
Примечание: (5) – отклонение от величины (ЗС) в процентах.
У больных всех групп данные закономерности были существенно нарушены. Характер и степень этих нарушений зависели от выраженности морфологических изменений мышцы сердца. Отчетливые отклонения от «ЗС» выявлены уже у больных 1 группы. По большинству показателей эти отклонения составляли 10-20%. Процент отклонений изучаемых показателей от цифр «ЗС» были в 2-4 раза больше, чем в контроле. Максимальные отклонения от пропорции «ЗС» наблюдались у больных 2 группы и составляли 15-50%, что примерно в 3-10 раз больше контрольных показателей. От «ЗС» больше всего отклонялись отношения систолического объема ЛЖ к ударному объему и пиковых скоростей диастолического кровотока.
У больных с ХСН (3группа) отклонения отношений изучаемых величин от «ЗС» достоверно не отличались от таковых у больных 2 группы. Более того, у них наметилась наклонность к уменьшению некоторых показателей: отношений толщины задней стенки, межжелудочковой перегородки в систолу и диастолу.
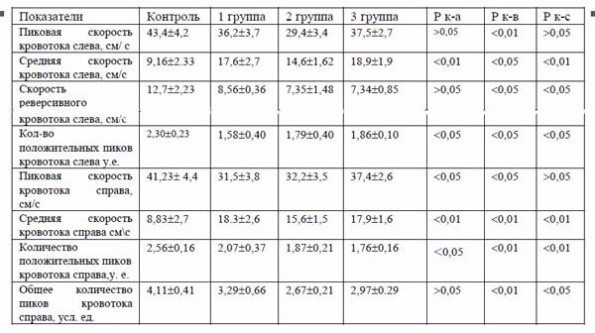
Таблица 4. Характеристика гемодинамики в плечевых артериях у больных ХСН
Одновременно с морфофункциональными изменениями в сердце у больных ИБС и ГБ выявлено нарушение кровотока по сосудам мышечного и эластического типа (сонные, плечевые и бедренные артерии) (Табл. 4) Эти нарушения в разных сосудах имели однонаправленный характер, хотя в количественной выражении они отличались друг от друга. В первую очередь следует отметить достоверное снижение пиковых скоростей кровотока по перечисленным артериям. Наибольшее снижение скорости кровотока наблюдалось у больных 2 и 3 групп, хотя достоверной разницы в показателях больных данных групп не выявлено.
Снижение скоростей кровотока по артериям сопровождалось падением минутного объема. Резкое снижение этого показателя по всем сосудам отмечено у больных 1 группы. У больных 2 и особенно 3 группы он несколько возрастал, достигая половины от контрольного (p < 0,001). На фоне снижения минутного объема происходило увеличение ударного объема. Наиболее отчетливо это проявилось у больных 1 группы, у которых он увеличился в 2 и более раза. У больных 2 группы ударный объем несколько снизился, а у больных 3 группы вновь увеличился. Количество положительных пиков кровотока уменьшилось, больше всего у больных 2 и 3 групп.
Таким образом, у больных ИБС и ГБ выявлено нарушение структуры миокарда, центральной гемодинамики и кровотока в крупных сосудах, которые усиливались по мере прогрессирования этих заболеваний.
Обсуждение и выводы
Полученные нами данные свидетельствуют о том, что патологический процесс в сердце начинается с повреждения морфологических структур и постепенно прогрессирует. Для поддержания насосной функции сердца организм использует компенсаторные реакции, которые на первых порах задействуют механизм Франка-Старлинга и гиперплазию органелл кардиомиоцитов. Это проявляется гипертрофией ЛЖ и умеренной дилатацией полостей сердца и соответствует тоногенной дилатации по Г.Ф.Лангу. За счет этого происходит восстановление, возможно, и усиление инотропной функции сердца, что обеспечивает нормальное кровообращение в органах и тканях. Данное положение подтверждается результатами исследования больных 1 группы, у которых установлено увеличение размеров и объемов ЛП и ЛЖ, признаки гипертрофии ЛЖ. У больных ГБ к ранним проявлениям следует отнести гипертрофию и дилатацию левого предсердия. По данным П.П. Ченрыша (10), эти изменения могут быть обусловлены увеличением объема циркулирующей крови.
Помимо изменений в структуре сердца у этих больных имеет место нарушение гемодинамики по сосудам эластического и мышечного типа в виде снижения пиковой скорости, скорости реверсивного кровотока, общего количества пиков кровотока и увеличения средней скорости кровотока.
Прогрессирование болезней сердца, с одной стороны, сопровождается дальнейшими морфофункциональными изменениями, с другой – включением все новых механизмов компенсации не только самого сердца, но и других систем, направленных на нейтрализацию и ликвидацию последствий разрушающего действия патогенных факторов.
Это отчетливо прослеживается на больных 2 группы, у которых отмечена наибольшая гипертрофия ЛП, межжелудочковой перегородки, ЛЖ, значительное увеличение полостей сердца (его ремоделирование), снижение ФВ, максимальное отклонение отношений структур и функций сердца от пропорции «ЗС», стойкого повышения А/Д. Однако насосная функция сердца у этих больных остается еще на достаточно высоком уровне, обеспечивая кровоснабжение организма в повседневных условиях. Необходимо подчеркнуть, что у больных 2-й группы уже можно выявить признаки скрытой сердечной недостаточности, о чем свидетельствует значительное увеличение размеров ЛП, ЛЖ, их объемов, времени изометрического расслабления, что соответствует первой стадии сердечной недостаточности по Ф.И. Комарову, Л.И. Ольбинской (9). По нашим данным, важными показателями начальных проявлений сердечной недостаточности является увеличение конечных систолического и диастолического объемов ЛЖ, систолического размера ЛЖ, а также соотношения КСР к КДР ЛЖ и особенно систолического объема к ударному. Отношение ударного объема ЛЖ к диастолическому (фракция выброса) хотя и отражает степень выраженности СН, но не является столь обязательным признаком этого осложнения.
Представленные данные позволяют предположить, что у больных 2 группы компенсаторные возможности сердца, связанные с его гипертрофией, практически исчерпаны, ибо она охватывает все мышечные структуры этого органа, а тоногенная дилатация ЛЖ сменилась на миогенную. Что это действительно так, подтверждают результаты исследования больных 3 группы, у которых наблюдаются явные признаки сердечной недостаточности. Оказалось, что большинство изучаемых показателей у них было таким же, как и у больных 2 группы. Разница между ними не существенна. Непременно возникает вопрос, почему же при одинаковых морфологических изменениях в сердце, у одних больных выявлялась явная сердечная недостаточность, у других она отсутствовала или проявлялась в скрытом виде.
Ответ на этот вопрос, на наш взгляд, могут дать данные об однонаправленноси изменений показателей, характеризующих мышечную массу с сердца. У больных 3 группы прослеживаются снижение массы миокарда, ИММ ЛЖ, уменьшение толщины задней стенки ЛЖ в систолу и диастолу, межжелудочковой перегородки. Эти данные говорят о том, что сердце у больных не способно дальше гипертрофироваться и таким образом компенсировать полностью насосную функцию. Гипертрофированная ткань обладает меньшими потенциальными возможностями, быстрее исчерпывает свой ресурс, погибает и замещается соединительной тканью, происходит постепенное склерозирование сердечной мышцы. Оставшаяся часть гипертрофированной мышцы сердца не способна выполнять инотропную функцию сначала при физической нагрузке, а затем и в покое. Выявленные нарушения кровотока по сосудам мышечного типа указывают на поражение всей сердечено-сосудистой системы и развитие сердечно-сосудистой недостаточности, или недостаточности кровообращения.
У больных 3 группы имело место включение в компенсаторный процесс, направленный на поддержание кровообращения в организме, других органов и систем. В частности, произошло усиление симпатического звена вегетативной нервной системы, что проявилось увеличением частоты сердечных сокращений. В процесс включились дыхательная система (появилась одышка), почки (задержка жидкости в организме), по-видимому, эндокринная система.
Представленные нами данные о последовательности развития морфофункциональных нарушений сердца и сосудов у больных ГБ и ИБС позволяют выделить два периода или две стадии течения патологического процесса независимо от того, чем он вызван (нагрузкой давлением или поражением коронарных артерий). Первая стадия характеризуется полной компенсацией инотропной функции сердца, что соответствует НКо по Г.Ф. Лангу или «А» стадии по классификации АСС/АНА. Для второй стадии свойственно истощение компенсаторных реакций, т.е. декомпенсация. Она может проявляться различной степенью выраженности. Так, выявленные изменения у больных 2 группы можно рассматривать как субкомпенсацию или первую степень декомпенсации, которая, как правило, выявляется при повышенной физической нагрузке. У больных 3 группы обнаруженные изменения можно отнести к 2 степени декомпенсации. Полная декомпенсация, или 3 степень, свойственна больным с клиническими признаками сердечной недостаточности, проявляющимися в покое.
На основании полученных данных можно сделать вывод, что ХСН есть проявление декомпенсации сократительной функции сердца и других систем организма. Степень выраженности функциональных нарушений отражает тяжесть сердечной недостаточности и прогрессирование патологического процесса, приведшего к ХСН. Она зависит, с одной стороны, от характера течения заболевания, и другой -- от компенсаторного потенциала организма. Чем выше этот потенциал, тем менее выражена ХСН. Проявления ее также будет уменьшаться при снижении активности патологического процесса спонтанно или под влиянием терапии. Рецидив болезни или неадекватное лечение приводит к нарастанию выраженности декомпенсации, а значит, и тяжести хронической сердечной недостаточности.
С этих позиций ХСН вряд ли можно отнести к нозологическим формам болезни только на том основании, что она развивается по единым патофизиологическим законам вне зависимости от этиологии повреждения. (1). В основе развития этого синдрома лежит патоморфологический процесс, завершающийся кардиосклерозом. Морфологические изменения мышцы сердца и компенсаторные возможности определяют степень выраженности функциональных нарушений деятельности сердца. Развившиеся нейрогуморальные расстройства есть проявления компенсаторных реакций других органов и систем, направленных на поддержание сократительной функции сердца и других систем жизнеобеспечения организма в целом.
ХСН – заключительная стадия (завершающий этап) различных заболеваний сердца. Она развивается у больных с нарушенными компенсаторными возможностями. ХСН, являясь стадией болезни, в принципе не может быть разделена на стадии, ибо они предполагают этапность протекания болезни, а не синдрома, и невозможность перехода от тяжелой стадии к более легкой. Хотя в течении ее и просматривается определенная стадийность, но она не является закономерной и в большей мере определяется прогрессированием основного заболевания. ХСН в значительной степени проявляется функциональными нарушениями деятельности сердечно-сосудистой системы. Выраженность этих нарушений может изменяться как в сторону улучшения, так и в сторону ухудшения в зависимости от характера течения основного заболевания, компенсаторного ресурса организма и от успешности проводимого лечения. Степень декомпенсации как проявление функциональных нарушений пораженного органа или системы отражает тяжесть течения процесса. Поэтому тяжесть ХСН целесообразно определять не стадией, а степенью функциональных нарушений или функциональных классов.
Учитывая тот факт, что в развитии сердечной недостаточности принимают участие нарушения периферического кровообращения, тканевой перфузии, метаболизма тканей (3), целесообразнее говорить о сердечно-сосудистой недостаточности, или недостаточности кровообращения, подразделяя ее на 3 или 4 степени тяжести либо функциональных класса.
Выводы: 1.Прогрессирование ИБС и ГБ сопровождается модификацией структуры сердца, нарушением центральной гемодинамики и периферического кровообращения.
2. Появление клинических симптомов ХСН обусловлено исчерпанием компенсаторных возможностей в виде гипертрофии мышцы сердца.
3. Ранними признаками ХСН являются увеличение конечного систолического объема левого желудочка, отношения его к ударному объему, а также скоростей наполнения левого желудочка.
Литература
- Беленков Ю.Н., Мареев В.Ю., Арутюнов Г.П., Агеев Ф.Т. Национальные рекомендации по диагностике и лечению ХСН. Журн. Сердечная Недостаточность. 2002; (3),6:3-19.
- Обрезан А.Г., Вологдина И.В. Хроническая сердечная недостаточность. СПб.: «Вита Нова»; 2002.
- Обрезан А.Г. к вопросу о терминологии: недостаточность кровообращения или «сердечная недостаточность»? // Медицина ХХI век, 2005; 1: 50-54.
- Кушаковский М.С. Хроническая застойная сердечная недостаточность. Идиопатические кардиомиопатии. СПб., Фолиант; 1998.
- Саркисов Д.С. Некоторые особенности развития медико-биологических наук в последнее столетие. Клин. мед.,2000; 8: 4-8.
- Структурные основы адаптации и компенсации нарушенных функций/ Под ред. Д.С. Саркисова. М.: Медицина; 1987.
- Малов Ю.С. Биологические основы здоровья и болезней. Вестн. Рос. Военно-медицинской академии. 2003; 2: 141-146.
- Меерсон Ф.З. Адаптация, дезадаптация и недостаточность сердца. М.: Медицина,1977.
- Комаров Ф.И., Ольбинская Л.И. Начальная стадия сердечной недостаточности. М.: Медицина, 1978.
- Черныш П.П., Малов Ю.С. Использование пропорций «золотого сечения» для диагностики хронической сердечной недостаточности. Кардиология СНГ, 2003; 1:312.
- ACC/ANA/ Guidelines for the Management of Patients With Chronic Heart Failure 2002// Internet source: www. Acc.org.
Резюме
Целью исследования явилось изучение механизмов развития ХСН у больных ИБС и ГБ. Обследовано 166 больных, которые были разделены на 3 группы в соответствии с классификацией АСС/АНА в зависимости от стадии ХМН «А», «В» и «С». Всем больным и здоровым проводились клиническое обследование, ЭХО-кардиография, суточное мониторирование ЭКГ, допплерография сонных, плечевых и бедренных артерий, изучались соотношения структур и функций отделов сердца по правилам «золотого сечения». У больных «А» стадии ХСН, т. е. при полном ее отсутствии, наблюдалась умеренная гипертрофия ЛЖ, незначительное увеличение конечных систолического и диастолического размеров ЛЖ, изменение соотношений размеров и объемов ЛЖ, нарушение кровообращения по крупным сосудам.
У больных «В» стадии ХСН выявлено дальнейшее нарушение центральной и периферической гемодинамики без субъективных признаков сердечной недостаточности. Изменения же структуры и функций сердца у больных 3 группы с явными симптомами недостаточности кровообращения мало чем отличались от таковых 2 группы. Выявленная тенденция к уменьшению массы, ИММЛЖ, толщины задней стенки ЛЖ у больных 3 группы позволяет предположить, что компенсаторные реакции в виде гипертрофии левого желудочка исчерпаны, что привело к нарушению насосной функции сердца и развитию сердечной недостаточности.
Источник: Малов Ю.С, Обрезан А.Г.Патогенез хронической сердечной недостаточности: новые механизмы развития \\ Медицина XXI век. - № 7 (8). – 2007. – С. 39-44.