Введение
В последние десятилетия в современной медицине интенсивно развиваются направления, связанные с исследованием структуры и функции органов и тканей. Приведенный процесс обусловлен, прежде всего, возрастающей потребностью практикующих врачей и исследователей в изучении организма человека на качественно новом уровне, более глубоком и функциональном, чем это было прежде. Действительно, методы диагностики и научного исследования, используемые в медицине рутинным образом (осмотр, пальпация, перкуссия, аускультация), разработанные и усовершенствованные нашими предшественниками, позволяют лишь предположить диагноз или проблему. Для уточнения всякого предварительного диагностического суждения используются многочисленные дополнительные методы. В основном, их можно разделить на две группы: методы, изучающие структуру и методы, исследующие функцию организма, системы, органа, ткани и т. д.
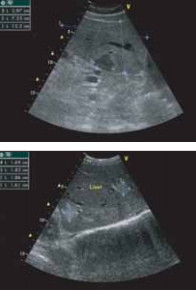
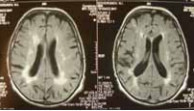
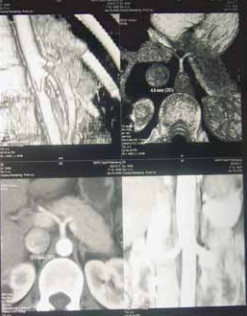
Для диагностики структурных изменений в органах и тканях традиционно широко применяют рентгенографию и рентгено-томографию. В последние десятилетия используются более точные методы исследования: ультразвуковое исследование (рис. 1), компьютерная томография (рис. 2), магнито- резонансная томография (рис. 3).
Рис. 1. Очаговые образования в ткани печени при ультразвуковом исследовании органов брюшной полости.
Рис. 2. Лейкоареоз Бенцвангера при компьютерной томографии головного мозга.
Рис. 3. Диагностика стеноза чревного ствола при магнито-резонансной томографии сосудов брюшной полости.
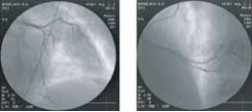
Для исследования состояния сосудов используются также ангиографические методики: флебография — для вен и ангиография — для артерий (рис. 4), сочетающие рентгенологические и контрастные методы визуализации.
Рис. 4. Коронароагниография.
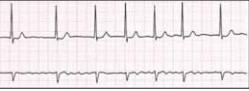
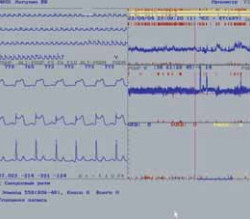
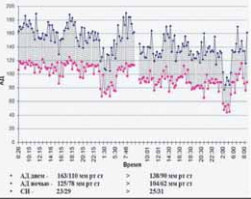
Функциональные изменения в органах и тканях изучаются с помощью методов функциональной диагностики: электрокардиографии (одномоментное исследование электрических процессов в сердце), (рис. 5); суточного мониторирования ЭКГ (длительное динамическое изучение электрической составляющей деятельности сердца) (рис. 6); суточного мониторирования АД (исследование динамики сосудистого тонуса) (рис. 7) и многих других.
Рис. 5. Фибрилляция предсердий при ЭКГ-исследовании.
Рис. 6. Эпизод стенокардии Принц-Металла при суточном мониторировании ЭКГ.
Рис. 7. Суточная мониторограмма артериального давления.
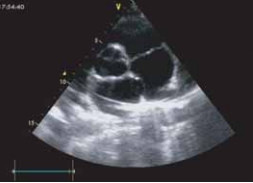
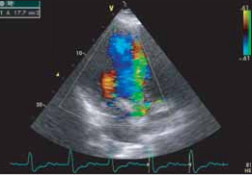
Многие современные диагностические методы сочетают возможности изучения структурных и функциональных составляющих организма человека. Так, эхокардиография позволяет получить не только морфометрические характеристики миокарда, полостей, клапанов сердца (размеры, эхоплотность и т. д.) (рис. 8), но и данные о динамических функциях сердца (сократимость, расслабление, скорости кровотока, характер потока крови и др.). (рис. 9).
Рис. 8. Аневризма овального окна при ЭХО-кардиографическом исследовании
Рис. 9. Выраженная аортальная регургитация вследствие отрыва некоронарной створки аортального клапана при цветном допплеровском картировании в рамках ЭХО-кардиографического исследования.
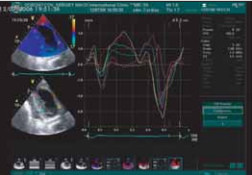
Более детальное представление о динамике тканевых процессов (в частности, метаболизм-зависимой кинетике миокарда) дает, так называемое TVI-исследование (tissue velocity imaging), часто сопровождающееся количественным анализом сократимости и расслабления миокарда (рис. 10).
Рис. 10. Исследование кинетики миокарда с использованием тканевой цветной допплерографии и количественного анализа.
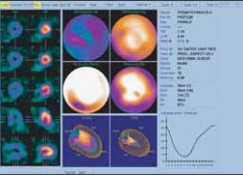
Еще одним примером сочетанных возможностей изучения структуры и функции органов и тканей может служить сцинтиграфия и позитронно-эмиссонная томография. Методы сцинтиграфии позволяют получать не только кривые транспорта индикатора или значения радиоактивности исследуемой области, но также изображение органов и тканей-мишеней, а результаты компьютерной обработки сцинтиграмм дают наглядное представление о распределении функциональных характеристик — так называемые параметрические изображения (рис. 11).
Рис. 11. Сцинтиграфия миокарда с процессинговым компьютерным моделированием сердца.
Перфузионная сцинтиграфия миокарда зарекомендовала себя как высокочувствительный неинвазивный метод диагностики жизнеспособного миокарда. Высокая степень включения (экстракции), равномерное распределение меченых атомов и вымывание (перераспределение) их из миокарда свидетельствует не только о нормальной перфузии, но и о целостности клеточных мембран и ненарушенной метаболической функции. Регионарное снижение захвата изотопа может отражать как обеднение коронарного кровотока, так и миокардиальный некроз или фиброз.
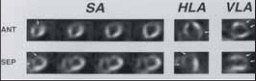
Сцинтиграфия с целью диагностики острого инфаркта миокарда основана на способности 99mТс-пирофосфата накапливаться в зоне некроза миокарда. Оптимальным сроком для исследования являются 2-7 сутки от появления симптомов инфаркта, который определяется на сцинтиграмме по очаговому характеру включения радиофармпрепарата (рис 12).
Рис. 12. Сцинтиграфия миокарда с технецием: стрелками показаны дефекты накопления радио-фармпрепарата при остром инфаркте миокарда. SA — короткая ось; HLA — горизонтальный срез по длинной оси; VLA — вертикальный срез по длинной оси; ANT — передняя стенка; SEP — перегородка; LAT — боковая стенка; INF — нижняя стенка ЛЖ.
Повторные исследования позволяют судить о динамике репаративных процессов, прогнозировать развитие процесса. Уменьшение или полное отсутствие включения РФП в миокард свидетельствует о благоприятном течении ОИМ, расширение зоны накопления РФП в миокарде — об отрицательной динамике.
Особенно значимо в диагностическом плане исследование, именуемое однофотонная эмиссионная томография. Исследование проводится с 99mТс-пирофосфатом (или с мечеными моноклональными антителами, тропными к поврежденному миокарду) и используется для оценки размеров инфаркта миокарда.
Изучение перфузии миокарда проводят с помощью нагрузочной сцинтиграфии сердца, которая позволяет оценить адекватность его кровоснабжения. Исследовать перфузию миокарда можно с помощью как планарной сцинтиграфии, так и однофотонной эмиссионной компьютерной томографии. При планарной сцинтиграфии изображения регистрируют в передней, левой косой и левой боковой проекциях, что позволяет визуализировать различные сегменты миокарда. При ОЭКТ изображения реконструируются в виде множества срезов в трех ортогональных проекциях: по короткой, горизонтальной длинной и вертикальной длинной осям ЛЖ.
Радионуклидные исследования перфузии миокарда обычно проводят в сочетании с нагрузочными пробами. В качестве нагрузочной пробы чаще всего применяют субмаксимальную нагрузку на велоэргометре, тредмил-тест, чреспищеводную стимуляцию или фармакологические пробы с вазодилататорами: дипиридамолом и аденозином или инотропным агентом добутамином. РФП вво- дят внутривенно на пике нагрузки, а исследование проводят через 5-10 мин. Классическим РФП для визуализации перфузии миокарда является таллий- 201(201Tl) с периодом полураспада 24 ч. Являясь биологическим аналогом калия, 201Tl после внутривенного введения распределяется в мышце ЛЖ пропорционально региональному миокардиальному кровотоку. Распределение 201Tl отражает распределение внутриклеточного калия, а его вымывание может быть оценено количественно и составляет в нормальных сегментах не менее 30% за 2,5-З часа после введения на пике нагрузки. Это последнее свойство может обеспечивать дополнительную информацию относительно клеточной жизнеспособности и позволяет идентифицировать сократительную дисфункцию жизнеспособного миокарда, возникшую вследствие хронической гипоперфузии миокарда. Пер- вичное распределение и последующее перераспределение 201Tl, отображающее в комбинации с фармакологическим стресс-тестом индуцированную коронарную гиперемию, способны идентифицировать следующие типы миокардиальной ткани: нормальная, ишемическая, инфарцированная и гибернация. После физического или фармакологического стресса происходит 2-4 кратное увеличение коронарного кровотока относительно базального уровня. Миокард, кровоснабжаемый нормальными коронарными артериями, поглощает большие количества 201Tl относительно поглощения в покое. Области миокарда, расположенные дистально от значимого стеноза коронарной артерии, не способны увеличить кровоток, и поглощение 201Tl после стресс-теста становится меньше исходного в сравнении с областями миокарда с нормальными или минимально измененными артериями. В области постинфарктного кардиосклероза или гибернирующего миокарда поглощение 201Tl отсутствует или минимально. Преходящая ишемия миокарда характеризуется наличием локального снижения накопления РФП на нагрузочных сцинтиграммах и замедленным клиренсом ишемизированного миокарда, благодаря чему на отсроченных сцинтиграммах через 4 или 24 ч изображение становится более равномерным (так называемый преходящий дефект перфузии). Таким образом, нагрузочные сцинтиграммы позволяют оценить реги
В последнее время в клиническую практику активно внедряются РФП, меченные 99mТc (технецием): сестамиби, тебороксим. Будучи аналогами таллия по сфере применения и обладая тем же основным свойством — линейной зависимостью между миокардиальным кровотоком и региональным включением индикатора, новые технециевые препараты имеют оптимальные физические свойства, дают меньшие лучевые нагрузки, отличаются по кинетике и некоторым методическим особенностям проведения исследования. Их применение позволяет определять адекватность кровотока, утолщение стенок левого желудочка, фракцию выброса.
Позитронная эмиссионная томография (ПЭТ) — современная технология радионуклидной диагностики, активно развивающаяся в последние годы. Основана на применении радиофармпрепаратов, меченных ультракороткоживущими изотопами (УКЖИ), которые являются позитронными излучателями. Большинство УКЖИ (18F, 11C, 15O, '14N и др.) представлено элементами, входящими в состав естественных метаболитов организма человека, поэтому ПЭТ предоставляет уникальные возможности для клинического изучения и оценки обменных процессов в органах и тканях, визуализации очагов патологической функциональной активности, дифференциальной диагностики морфологически близких поражений, оценки эффективности лечебных мероприятий.
Основными направлениями ПЭТ в кардиологии являются оценки локального миокардиального кровотока, регионарного метаболизма миокарда и локальной механической функции сердца. Метод применяется для диагностики локальной ишемии, оценки жизнеспособности миокарда, топической и дифференциальной диагностики областей с различной глубиной структурно-метаболических нарушений, обоснования показаний к оперативному лечению при ИБС, дифференциальной диагностики кардиомиопатий, оценки репаративных процессов в миокарде и жизнеспособности трансплантатов.
ПЭТ позволяет получать наиболее точную количественную информацию о региональной перфузии и метаболизме миокарда. Перфузия может быть оценена с помощью изотопов N-13 аммония, 15 0-Н2О, К-38 или Rb-82. Окислительный метаболизм обычно исследуется при применении С-11 ацетата, а утилизация глюкозы — при использовании F-18 флюородеоксиглюкозы (ФДГ). В настоящее время более распространено одновременное применение двух разных изотопов, позволяющих оценивать метаболизм и перфузию: ФДГ и N-13 аммония. Классические признаки несоответствия перфузии и метаболизма лежат в основе ПЭТ-диагностики жизнеспособного миокарда и являются наиболее точной его характеристикой. Было доказано также, что утилизация глюкозы достоверно выше в сегментах с восстанавливаемой после реваскуляризации сократимостью в отличие от сегментов без улучшения сократительной функции.
Несмотря на кажущееся многообразие представленных методов, диагностические потребности практикующих врачей и исследовательский интерес диктуют необходимость более глубокого проникновения в сущность биологических процессов, происходящих на уровне клетки, отдельного вида обмена веществ. Для исследования динамических процессов в возбудимых тканях человеческого тела, например, в миокарде, гладкой мускулатуре сосудов используются в основном физические механизмы визуализации этих явлений. Это такие подходы как: электрофизиологические исследования, введение флюоресцентных красителей и др.
Одним из основных вопросов фундаментальной медицины и клинической практики является определение инициативных процессов в пейсмекерных клетках и триггерных зонах возбудимых тканей. Главная и самая сложная задача визуализации заключается в том, чтобы отдифференцировать интересующий процесс от других параллельных явлений, происходящих в исследуемых тканях. Разрешение этой задачи в медицине упирается в необходимость селективного введения маркеров в исследуемые клеточные структуры. Современным достижением науки является возможность использования для этой цели полупроводниковых квантовых точек.
В перспективе использование квантовых точек представляется пригодным для изучения любых статических и динамических процессов в тканях организма, в частности: кинетики ферментативных процессов, роста и развития опухолевых клеток.
Физическая природа квантовых точек
Полупроводниковые квантовые точки достаточно эффективно используются в опто- и наноэлектронике [1, 2]. Отдельная квантовая точка представляет собой специальным образом полученный наноразмерный объект, обладающий дискретным энергетическим спектром. Способы получения полупроводниковых квантовых точек весьма различны: они могут создаваться из планарных полупроводниковых гетероструктур с помощью литографии, могут получаться химическими методами, но наиболее широко распространенным способом получения квантовых точек является спонтанное формирование наноразмерных островков-включений одного полупроводникового материала в матрице другого. Носители заряда оказываются локализованы в пределах островка, следствием чего и является квазиатомный (представляющий собой набор отдельных уровней) энергетический спектр. Благодаря этой особенности квантовые точки обладают рядом достоинств с точки зрения практического применения: на их основе сейчас создаются как новые виды полупроводниковых лазеров, так и принципиально новые устройства (например, источники одиночных фотонов для квантовой криптографии).
С увеличением радиуса квантовых точек от 50 до 200 А длина волны излучения увеличивается от 400 до 103 nm. В отличие от других флуоресцентных систем, полупроводниковые квантовые точки имеют пороговую энергию возбуждения, поэтому их можно возбуждать и этой, и большей энергией. Таким образом, пороговая энергия не должна совпадать с энергией излучательного перехода внутри квантовых точек. Это позволяет возбуждать на одной длине волны многие квантовые точки, каждая из которых излучает на своей собственной длине волны.
Благодаря наличию узких и симметричных пиков излучения полупроводниковые, квантовые точки могут быть использованы для оптической диагностики, при которой получение пиков на разной длине волны и разных интенсивностей может быть использовано для идентификации генов, аминокислот, белков и молекулярных цепочек.
Одна из наиболее распространенных технологий роста полупроводниковых гетероструктур вообще и квантовых точек в частности — молекулярно-пучковая эпитаксия. В этой методике выращивание пленок или более сложных структур производится в высокова- куумной установке путем осаждения атомов (или молекул) испаряемого (-ых) вещества (-ств), содержащегося (-ихся) в специальном (-ых) источнике (-ах), на поддерживаемую при заданной температуре подложку. Однако на свойства получающихся структур влияет множество факторов (температура подложки, потоки вещества из источников, свойства осаждаемых материалов, кристаллическое совершенство подложки и т. д.) (рис. 13).
Рис. 13. Топология квантовой точки, полученная при помощи электронного микроскопа.
Применение квантовых точек в медицине
В настоящее время установлено, что полупроводниковые квантовые точки находят новое применение в биологии и медицине [3-5]. В первую очередь, квантовые точки используются как новые инструментальные средства для получения изображения и диагностики живых клеток в естественных условиях. Как показано в ряде работ [3, 4], квантовые точки обладают лучшими свойствами, чем флуоресцентные хромофоры, которые в настоящее время используются в биологии и в медицине, например, для картирования сердца [6], а именно: а) более высоким квантовым выходом излучения, б) оптической активностью в длинноволновой области спектра и в) значительно большей фотохимической стабильностью. Оптические свойства квантовых точек существенно зависят от их размеров.
Применение квантовых точек в флуоресцентной интроскопии организма имеет ряд преимуществ по сравнению с традиционными методами: во-первых, они, в отличие от традиционных химических красителей, не подвержены обесцвечиванию (уменьшение интенсивности флуоресцентной эмиссии при облучении молекулы красителя источником света), во-вторых, интенсивность свечения квантовых точек примерно в 3000 раз сильнее, чем у обычных красителей. Таким образом, уникальные спектральные свойства квантовых точек являются весьма перспективными для исследований в биотехнологии и медицине.
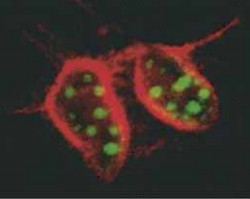
В ряде работ описана разработка многофункциональных проб на основе полупроводниковых квантовых точек для детектирования раковых клеток в живых организмах и для получения изображения этих клеток [4, 5]. Изу- чение роста клеток раковых опухолей у животных показало, что квантовые точки накапливаются в опухоли как за счет улучшенной проницаемости, так и за счет присоединения к поверхности биомаркеров раковых клеток по механизму антител. Были получены высококачественные цветные изображения раковых клеток непосредственно в живом организме [5] (рис. 14). Тем самым, с помощью квантовых точек продемонстрированы новые возможности для получения изображений молекулярных объектов в живом организме с высокой чувствительностью.
Рис. 14. Визуализация клеток опухоли с помощью квантовых точек.
В работе [7] подробно рассмотрен вопрос о применении квантовых точек для диагностики патологии обмена аминокислот. Поскольку аминокислоты являются фундаментальной составляющей всех белков организма, это актуально для исследования кинетики биохимических процессов в здоровых и патологически измененных тканях человека.
Принцип действия и основные проблемы использования квантовых точек
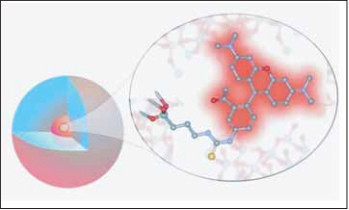
Квантовая точка, как уже говорилось, является оптическим маркером. Для того чтобы селективно визуализировать те или иные ткани, ее необходимо химически связать с клетками этой ткани таким образом, чтобы, во- первых, эта химическая связь не влияла на естественный ход процессов в клетках и тканях функциональной структуры, а во-вторых, обеспечить химический способ связи с высокой аффинностью к клеткам исследуемой ткани. На рис. 15 показана схема такого взаимодействия [8].
Рис. 15. Пример химического соединения квантовой точки с клеткой.
Теоретически обоснованный способ визуализации структурно-функциональных перестроек в органах несет в себе еще одну возможность. Введение квантовых точек с различным спектром фотолюминесценции в функционально разные слои тканей одного и того же органа позволяет одновременно визуализировать сразу несколько параллельных процессов. При этом, в ряде случаев можно выявить причинно-следственную связь про- исходящих явлений в исследуемых регионах. Таким образом, появляется возможность дифференцировать первичные нарушения и сопровождающие их вторичные изменения.
Кроме изучения динамики макромолекулярных процессов в тканях и органах, определенные типы квантовых точек позволяют регистрировать субмолекулярные перестройки на клеточном уровне. Достигается это за счет того, что химическое окружение в ряде случаев оказывает влияние на спектр люминесценции квантовой точки.
На организменном и макроуровне перспективным представляется также использование квантовых точек в диагностике диффузных и очаговых воспалительных заболеваний миокарда, кардиомиопатий, миокардиодистрофий, для уточнения природы которых в современной медицине нет ни одного адекватного метода. Насущной потребностью является и необходимость отслеживания миграции, «хоуминга», дифференциации и последующего функционирования так называемых стволовых клеток, на которые возлагаются огромные надежды в плане репаративной и регенеративной терапии некурабельных заболеваний. Так, перспективы доказательства закрепления стволовых мезенхимных клеток в «целевом органе» после системного или даже локального введения ограничиваются возможностями экспериментального плана (на животных) с использованием флюоресцентных меток и необходимостью последующего секционно-микроскопического изучения. Метить недифференцированные клетки-предшественники радио- нуклидными препаратами не представляется возможным ввиду опасности их гибели вследствие радиоактивного излучения и недостаточности периодов полураспада радиофарм-препаратов. Говорить о наблюдении процесса дифференцировки и последующей интеграции в метаболизм ткани и органа также не представляется возможным на современном этапе. Именно в указанной связи применение технологии «квантовых точек» представляется весьма привлекательным.
Заключение
Приведенные в статье описания методов исследований в современной медицине, разумеется, не претендуют на исчерпывающий перечень диагностических и научных подходов. Тем не менее, представляется исключительно перспективным развитие диагностических направлений именно функционального плана. На основании изложенного, представляется целесообразным использование полупроводниковых квантовых точек в двух принципиально различных диагностических направлениях. Первое — исследо- вание динамических процессов. В этом случае квантовые точки используются как оптические метки векторных взаимодействий в тканях. При этом внешняя по отношению к квантовой точке молекулярная среда не оказывает на нее воздействия, таким образом, спектр люминесценции не меняется. Второе — квантовая точка выполняет роль лакмусовой бумажки по отношению к изменению химического и биофизического состояния исследуемой среды по сравнению с нормой. За счет химических взаимодействий спектр фотолюминесценции меняется, выявляя структурно-функциональные изменения быстрых и медленных перестроек в клетках тканей.
Необходимо особо подчеркнуть, что квантовые точки предоставляют возможность исследования и фундаментальных процессов в клетках, органах, тканях и целом организме, ими можно маркировать лиганды, гормоны, нейротрансмиттеры и, таким образом, изучать естественные взаимодействия химических сигналов с мембранами клеток.
Литература:
1. Асрян Л. В., Сурис Р. А. // ФТП, 2004, т. 38, в. 1, с. 325.
2. Леденцов H. Н. Устинов В. М., Егоров А. Ю. и др. // ФТП, 1994, т. 28, в. 8, с. 1483.
3. Warren C. W. et al. // Science, 1998, V. 281, P. 2016 2018.
4. Michalet X., Pihaud F. F., Bentolila L. A. // Science, 2005, V. 30, P. 538 544.
5. Xiaohu Gao, Yuanyuan Cui, Richard M. Levenson et al. // Nature Biotechnology, 2004, V. 22, N2, P. 969 974.
6. Розенштраух Л. В. Материалы школы «Совр. курс лекций по кл. физиологи». МГУ, 2006.
7. Зегря Г. Г. ПЖТФ. 2006, т.32, вып. 4, с. 75-81.
8. Steele В., Cornell University news notice, 19.05.2005.
9. Jean-Louis Viovy, // Rev. Mod. Phys. 2000. V. 72. N 3. P. 813-872.
10. Wen G. W., Lin J. Y., Jiang H. X., Chen Z. // Phys. Rev. B. 1995. V. 52. N 8, P. 5913-5922.
11. Покутний С. И. // ФТП, 2000, т. 34, в. 9, с. 1120- 1124.
12. Pokutnyi S. I, Jacak L., Misiewicz J., Salejda W., Zegrya G. G. // J. Appl. Phys., 2004, V. 96, N2, P. 1115-1119.
Источник: Обрезан А.Г., Ерофеев Н.П., Вчерашний Д.Б., Зегря Г.Г. Методы визуализации в клинике: использование квантовых точек для изучения динамических физических процессов // Журнал "Медицина XXI век № 3 {4} 2006" с. 49-52